公司新闻
Company News
专题笔谈·造血干细胞微移植 | 微移植治疗急性髓系白血病免疫机制
发布时间:2024-07-16 I 作者:中国实用内科杂志
急性髓系白血病(acute myeloid leukemia,AML)是一种常见的血液系统恶性肿瘤,以外周血、骨髓和(或)其他组织中髓系母细胞克隆性扩增为特征。AML最常见于65~74岁的老年人群,新诊断患者的中位年龄为68岁,超过一半(57.4%)的新诊断患者年龄≥65岁,其病死率在75~84岁人群中最高。随着强化诱导化疗和异基因干细胞移植(alloHSCT)的优化,65岁以下AML患者的中位总生存(OS)已显著改善,但老年、一般状况差以及具有不良风险疾病特征的患者因耐受较差,其OS仅略有改善[1-3]。新的化疗药物及靶向药物提供了患者完全缓解(CR)率,延长患者短期生存期,但长期疗效仍有争议。异基因造血干细胞移植配型要求较高,且毒性强、并发症较多,需服用移植物抗宿主病(GVHD)预防药物[4]。
这些问题使异基因造血干细胞移植在临床中应用中受限。微移植技术为老年及耐受较差的AML患者的治疗提供了新策略,其安全性和有效性已被证实,临床上简便易行,具有微毒高效的特点。微移植是一种化疗联合异基因造血干细胞输注的新的治疗方案,在患者接受预处理化疗后尽可能清除肿瘤细胞后输注粒细胞集落刺激因子(G-CSF)动员的外周造血干细胞,输注后供者体内形成微嵌合体,产生供者和受者抗白血病效应,加快血液学恢复,减轻感染、GVHD等并发症。微移植有效的确切机制并不十分清楚,大多认为可能与免疫效应有关,本文将对微移植免疫机制进行综述。
微移植是指将人类白细胞抗原(HLA)部分匹配或完全不匹配的供者的外周血干细胞(PBSCs)在没有或最小程度免疫抑制的情况下,输注给接受高剂量化疗或放疗的患者。这种方法的目的是利用供者的免疫系统对患者的白血病细胞进行攻击,从而实现治疗效果。
1.1 微移植的提出
在微移植技术提出之前,有研究就观察到,输注G-CSF动员的供者外周血干细胞(G-PBSCs)可增强移植物抗白血病效应(Graft-versus-Leukemia,GVL),并在不增加GVHD的情况下加快造血恢复[5-7]。艾辉胜教授团队在国际上率先提出微移植理念,动物实验表明,未经免疫抑制预处理的阿糖胞苷化疗后输注高剂量G-CSF动员的同种异体脾细胞的小鼠在未发生GVHD的基础上展现出快速的造血恢复和持续的微嵌合状态。在此基础上艾辉胜教授团队设计了一项临床对照研究,探讨G-PBSC输注联合常规诱导或强化缓解后化疗对老年AML患者预后的影响,于2011年在Blood首次发表,并证实其安全、有效[8]。
微移植是一种利用同种异体反应根除血液系统恶性肿瘤而不存在GVHD风险的新的移植模式,其设计理念主要有:(1)预处理:主要目的是在保留患者免疫功能的同时清除白血病细胞,应用包括常规剂量(非经典移植剂量)的化疗药物、去甲基化药物和(或)分子靶向药物等,以保留受者恢复免疫功能的能力。(2)供者细胞输注:预处理后输注来自HLA部分相合或完全不相合、亲缘或无关供者的异基因动员的G-PBSC,其中应用G-CSF动员的细胞很重要。(3)供体微嵌合及抗肿瘤作用:供体微嵌合状态可能持续或短暂,而不是完全供体嵌合。微嵌合体的形成可诱发移植物抗肿瘤效应(GVT)和宿主抗肿瘤(RVT)效应。(4)造血恢复快:非清髓治疗利于受者造血恢复,降低感染等并发症发生概率,有效提供患者生存率。(5)避免GVHD的风险:无需服用GVHD预防药物[9]。不难看出,微移植过程中免疫效应贯穿始终,发挥着重要作用。有效[8]。
1.2.1 微移植在AML中的临床应用
第一项关于MST的随机临床研究报道了在老年AML患者中比较常规化疗联合或不联合MST的结果,共计58例年龄超过60岁的患者被纳入,一组接受单独标准诱导化疗,另一组接受HLA不匹配的亲属G-PBSC输注[8]。结果MST组完全缓解率和2年OS率显著高于化疗组,且MST组患者造血恢复更快,没有观察到GVHD。这些结果首次证明了MST治疗老年AML患者的有效性和安全性。一项国际多中心回顾性报告,共纳入12个中心共185例患者,发现75~85岁的高龄患者也可从MST治疗中获益[10]。这些研究均证实MST对AML老年患者具有较好的疗效和安全性。
Sung等[11]报道17例接受MST治疗的老年AML患者,其中71%为高危患者,结果显示,所有低中危以及50%的高危AML患者(共62.5%)达到完全缓解。一项小样本前瞻性研究评估了23例初诊老年AML患者MST治疗疗效,90.9%的正常核型患者和80%的不良核型患者获得完全缓解。这些试验证实了MST对AML高危人群治疗的有效性。
Guo等[12]的一项研究纳入了101例首次完全缓解的AML患者,患者年龄分布在9~65岁,在接受3个周期的大剂量阿糖胞苷化疗后输注G-PBSC,未进行GVHD预防。结果显示低危组和中危组患者的6年LFS率分别为84.4%和59.2%,6年OS率分别为89.5%和65.2%。本中心自2015年开展微移植治疗AML,取得了相似的结果。
虽然多个研究已经证实了MST在治疗AML的有效性和安全性,但在微移植治疗中,复发仍然是主要问题。深入认识微移植作用的确切机制、应用优化的预处理方案、降低复发率和提高LFS率是进一步研究的重点。我们最新研究发现,在精细免疫指标指导下,优化应用BCL-2抑制剂——维奈克拉等微移植预处理方案,在治疗AML中起到更好的疗效。同时我们发现,经优化后预处理方案治疗后的患者精细免疫指标明显改善,提示微移植免疫机制在治疗AML中至关重要。
1.2.2 微移植在其他血液恶性肿瘤中的应用
在MST治疗AML的研究基础上,Hu等[13]将43例中危或高危骨髓增生异常综合征(MDS)合并tAML患者纳入研究,结果显示,经MST治疗后MDS组和tAML组CR率分别为52.4%和36.4%,2年OS分别为84.7%和34.1%。中性粒细胞的中位恢复时间分别为14 d和16 d,血小板的中位恢复时间分别为17 d和19 d。这些结果提示MST能使高危MDS或tAML患者获益。
10例复发和难治性淋巴瘤患者接受化疗联合G-PBSC输注4个周期,结果显示,6例CR,1例部分缓解(PR)。获得CR的患者随访29.5个月,均存活且无复发,2年OS和无病生存率均为60%[14]。
综上所述,MST在临床上有望广泛用于治疗各种血液系统恶性肿瘤。各类血液系统恶性肿瘤相关的MST临床研究也在进行中。
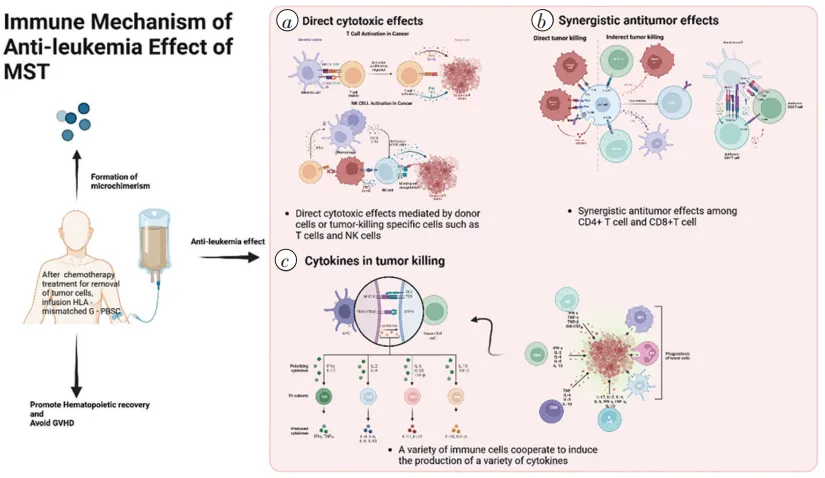
目前已被研究的MST作用机制中,免疫机制(见图1)占有重要地位,接下来将就微移植相关机制中的免疫机制着重阐述。
MST抗白血病作用可能与以下免疫机制相关:a. 供者细胞或肿瘤杀伤特异性细胞如T细胞、NK细胞介导的直接细胞毒性作用;b. 供者CD4+T细胞、CD8+T细胞协同抗肿瘤作用;c. 多种免疫细胞协同作用诱导产生多种细胞因子,产生受者抗白血病(GVL)效应
图1 微移植抗白血病效应免疫机制
2.1 微嵌合体在MST中的免疫作用
微嵌合体是指具有遗传差异的两个个体之间,其中某个体的微量细胞或DNA成分在另一个体内存在的状态。研究表明,微嵌合体具有免疫监视恶性细胞的功能,具有一定的抗肿瘤效应[15]。人体器官移植与微嵌合体有关,即在受者的不同器官中检测到供体细胞[16]。接受微移植的患者体内并未发现长期的供者细胞植入,但检测到短暂或持续的供者微嵌合(植入水平低于临床标准),因此不产生GVHD,但仍可检测到GVL效应[8,12]。微嵌合体的持续时间从几天到34个月不等,供者微嵌合体在移植后第2天出现,在移植后第7~14天达到高峰,最长持续时间为1020 d[12]。Sun等[17]发现微移植后在造血恢复的同时短时间内可检测到微嵌合体,提示微嵌合体可能加速造血恢复。微移植后产生的微嵌合体属于医源性微嵌合体,但微嵌合体在微移植中的功能作用机制尚未完全研究清楚,推测其具有一定的GVL效应且不产生GVHD。
Kliman等[18]开发了一种高度敏感的微滴数字PCR检测方法,可在临床用于精确定量嵌合体,包括检测限为0.008%和定量限为0.023%的微嵌合体,具有灵敏度高、重复性好等优点,是一种理想的监测手段。此外,其他如二代基因测序及单细胞测序等为微嵌合体的检测提供了更为灵敏的检测方法,有助于微嵌合体的进一步研究[19]。
2.2 抗白血病免疫效应
研究发现,输注高剂量供者CD3+T细胞(≥1.1×108/kg)患者的6年LFS和OS分别为76.4%和82.1%,显著高于输注低剂量供者CD3+T细胞(<1.1×108/kg)患者的6年LFS和OS(分别为49.5%和55.3%)[12]。这表明输注供者CD3+T细胞的剂量与存活率呈正相关,意味着输注供者T细胞在MST治疗中具有重要作用。这项研究还显示,39例HLA-A*02∶01抗原阳性患者中有33例WT1+CD8+T细胞显著增加(从0.2%增加到4.56%),提示产生了GVL和(或)受着抗白血病效应(RVL)效应。Wang等[20]通过建立小鼠白血病微移植模型,研究CD4+T细胞和CD8+T细胞对IFN-γ和IL-4释放的影响,结果表明IFN-γ在微移植小鼠抗白血病反应中起关键作用,CD4+T细胞计数与疗效呈正相关(r=0.722)。此外,观察到CD4+T细胞协同CD8+T细胞释放大量IFN-γ。提示T细胞协同释放IFN-γ是微移植治疗产生抗白血病免疫效应的重要环节。该实验还显示,IL-2对MST的抗白血病效应有进一步的增强作用。多项研究表明,供者及受者T细胞在MST发挥抗白血病免疫效应中发挥着重要作用。
Hu等[21]对131例完全缓解后低危和标危AML患者行MST治疗后NK细胞表面杀伤细胞免疫球蛋白样受体(KIR)和供受者间配体错配情况进行研究,结果显示,不同KIR配体的受者中位LFS显著高于相同KIR配体的受者。证实MST增强供者与受者NK细胞的效应,促进抑制性KIR活化,触发了NK细胞杀伤功能。不同KIR配体的受者的中位LFS显著高于相同KIR配体的受者。表明NK细胞的杀伤作用在MST抗白血病效应中至关重要。
我们的研究也发现,接受MST治疗的AML患者的NK细胞、总B细胞、Treg等细胞比例与接受传统化疗的患者之间具有显著差异,且经MST治疗的患者和未接受MST患者之间的总T细胞、CD4+T细胞、Treg、IL-17A、IFN-γ、IL-2的变化具有明显差异,证实MST的抗白血病效应中免疫细胞及细胞因子起着重要作用。我们的研究还显示,在疗效更优的优化预处理方案中,患者的免疫指标显著改善,其中CD4+T细胞、NK细胞、Treg以及12项细胞因子在MST中发挥重要作用,具体免疫机制正在进行深入研究。
2.3 血液学恢复与免疫重建
虽然MST治疗后造血功能恢复的机制尚不明确,但艾辉胜教授团队研究发现,在MST小鼠模型中观察到受体来源的linckit+sca1+细胞亚群从MST治疗后第1天的0.15%增加到第10天的1.9%,认为lin-ckit+sca1+细胞亚群增殖与造血恢复有关[9]。血液学造血恢复发生在供者微嵌合体的形成,表明微嵌合体和造血恢复之间的紧密关系。微嵌合体分泌的细胞因子可以在受者体内检测到,并在宿主体内发挥一定的功能。因此,供者细胞分泌的细胞因子可能具有加速造血恢复的作用。
Hu等[22]检测并分析T细胞的免疫功能和T细胞受体(TCR)文库。通过采用二代测序方法进行T细胞受体谱分析,结果显示,MST组总T细胞比例、γ/δT细胞、CD4+和CD8+T细胞水平高于单纯化疗组。MST治疗后半年和1年时,患者TCR呈多克隆性表达,表达相对均匀,提示免疫功能恢复较快,患者免疫功能的恢复或许与MST抗白血病免疫效应有关,并促进造血恢复。这些结果提示MST造血功能和免疫功能恢复紧密相关。
MST作为一种创新的移植和细胞治疗模式为AML患者的治疗提供了新方案,尤其是老年或不适宜于经典移植的AML患者,其较好的疗效及较少的副反应已被证实。微移植治疗AML的免疫机制涉及多个方面,包括GVL效应、免疫重建、GVHD的调控以及免疫微环境的改善。这些机制共同作用,使微移植成为治疗AML的有效方法之一。微移植有望为AML乃至其他血液肿瘤患者提供更多的治疗机会。未来的研究需要进一步揭示微移植的具体免疫机制,并探索更有效的方法来提高治疗效果和患者的生存质量。
参考文献(略)
ICP备字:京ICP备18062882号 © 2024 Copyright by INNOVVY All Rights Reserved.